肠道菌群 ×T 细胞:这对 “黄金搭档” 如何维持身体平衡?
本文将通俗解读肠道菌群如何通过分泌特殊物质、传递信号,调控 T 细胞的发育、功能,以及这对 “搭档” 失衡时如何引发炎症性肠病、乳糜泻等疾病,最后揭秘如何通过调节菌群改善健康的潜在方法。

你可能不知道,肠道不只是消化器官,更是人体最大的免疫器官 —— 肠道黏膜上布满了免疫细胞,时刻警惕着外来病原体。而这片 “免疫战场” 上,还生活着一个庞大的 “微生物乐园”—— 肠道菌群,它们包含细菌、真菌、病毒等,其中拟杆菌门和厚壁菌门占了总量的 90%。
这些微生物和人体形成了 “互利共赢” 的共生关系:菌群帮我们发酵膳食纤维产生短链脂肪酸(SCFAs)、合成维生素 B12 和 K,还能抵抗有害病菌;我们则为它们提供稳定的生存环境和营养。更关键的是,菌群还能 “训练” 免疫系统,教会它区分 “朋友”(自身细胞、有益菌群)和 “敌人”(致病菌、过敏原),而 Tregs 就是这场 “训练” 中最核心的 “学员”。
调节性 T 细胞(Tregs)是 CD4+T 细胞的一个特殊亚型,因表达转录因子 Foxp3 而具有强大的免疫抑制功能,就像免疫系统的 “和平使者”—— 它们能分泌 IL-10、TGF-β 等抗炎细胞因子,抑制过度的炎症反应,防止免疫系统 “误伤” 自身组织。
Tregs 主要分两类:在胸腺发育成熟的胸腺 Tregs(tTregs),负责预防自身免疫病;在肠道等外周组织分化的外周 Tregs(pTregs),专门介导对食物成分、肠道菌群等无害物质的耐受。尤其是肠道黏膜中的RORγt+Tregs,它们大多是外周来源,是维持肠道免疫平衡的 “主力军”,而它们的发育和功能,几乎完全依赖肠道菌群的调控。
肠道菌群对 Tregs 的调控,靠的是一套 “组合拳”,核心有三大 “法宝”,每一种都能精准影响 Tregs 的发育和功能。
菌群的细胞壁、荚膜等结构成分,能直接作为 “信号分子” 激活免疫细胞,进而调控 Tregs。比如:
多糖 A(PSA):来自人类共生菌脆弱拟杆菌的荚膜多糖,能通过结合 T 细胞表面的 TLR2 受体,直接诱导 Tregs 增殖,同时抑制促炎的 Th17 细胞,减少肠道炎症。
细胞表面 β- 葡聚糖 / 半乳聚糖多糖(CSGG):双歧杆菌的表面多糖,可激活肠道树突状细胞(DCs)产生抗炎因子,进而促进 pTregs 分化,增强其抑制炎症的能力。
甘露聚糖 /β-1,6 - 葡聚糖多糖(MGCP):来自酿酒酵母等真菌的细胞壁成分,能通过 Dectin-1 和 TLR2 双通路,一边诱导 Tregs 生成,一边抑制促炎的 Th1 细胞,双重守护肠道平衡。
这些结构成分就像菌群给免疫系统的 “通行证”,告诉 Tregs“我是朋友,不用攻击,还需要你帮忙维持秩序”。
菌群分解食物产生的代谢物,是调控 Tregs 的 “核心武器”,其中最关键的有三类:
膳食纤维经菌群发酵产生的乙酸、丙酸、丁酸,不仅是肠道细胞的能量来源,更是 Tregs 的 “成长激素”。它们能通过两种方式调控 Tregs:
结合免疫细胞表面的 GPR43、GPR109A 等受体,激活信号通路,促进 Tregs 增殖和功能强化;
直接抑制组蛋白脱乙酰酶(HDAC),增强 Foxp3 基因的表达,让 Tregs 更稳定、更 “能干”。
研究发现,缺乏 SCFAs 的小鼠,肠道 Tregs 数量会显著减少,更容易患上炎症性肠病;而补充 SCFAs 能有效恢复 Tregs 功能,缓解炎症。以下是常见的 SCFA 产生菌:
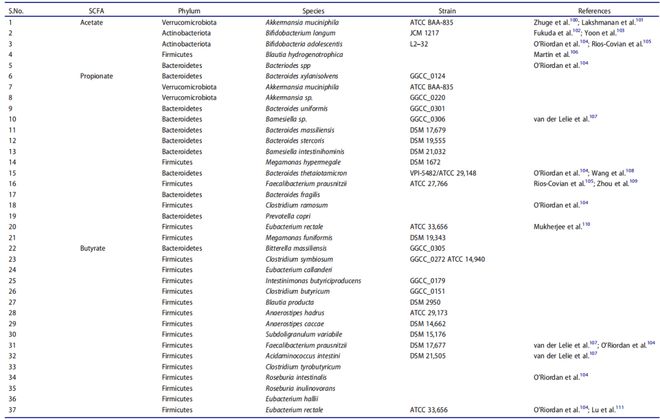
色氨酸是人体必需氨基酸,经菌群代谢后会产生吲哚、血清素等衍生物,它们能通过激活芳香烃受体(AhR),促进 Tregs 分化并增强其肠道归巢能力,让 Tregs 精准到达肠道发挥作用。比如血清素不仅能调节情绪,还能抑制 T 细胞的 mTORC1 通路,推动其向 Tregs 转化,尤其在婴幼儿期对建立免疫耐受至关重要。
肝脏合成的初级胆汁酸,经肠道菌群转化后生成次级胆汁酸(如脱氧胆酸、石胆酸),它们能通过 FXR、VDR 等受体,调控 Tregs 和促炎细胞的平衡。比如次级胆汁酸衍生物 isoalloLCA,能通过激活 Nr4a1 信号,增强 Foxp3 表达,让 Tregs 更稳定;而 3-oxoLCA 则直接抑制 Th17 细胞分化,减少炎症竞争。

肠道菌群的抗原能被树突状细胞(DCs)、3 型固有淋巴样细胞(ILC3)等抗原呈递细胞捕获,进而诱导 naive T 细胞分化为 pTregs。这些 pTregs 能精准识别菌群抗原,形成 “菌群特异性耐受”—— 既不攻击有益菌群,又能及时抑制针对菌群的异常炎症反应。
研究发现,婴儿期是菌群诱导 pTregs 的 “关键窗口期”,此时菌群紊乱会导致 pTregs 发育不良,成年后更容易患上过敏性疾病或自身免疫病。
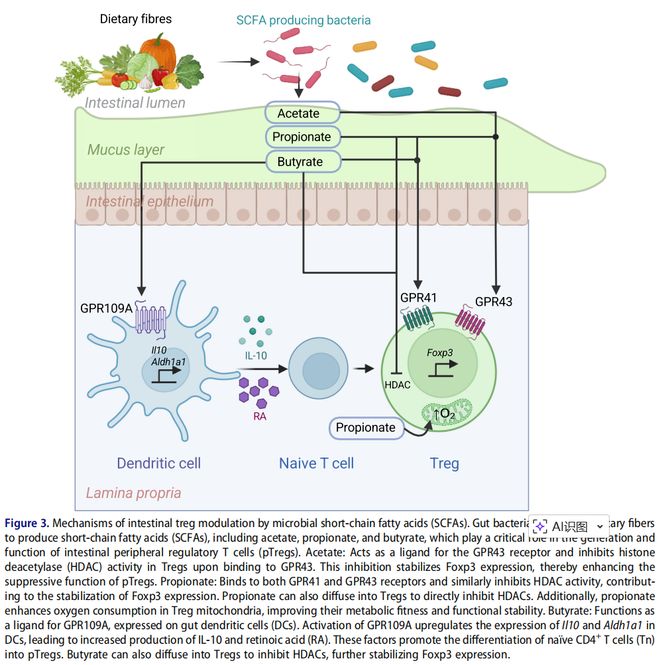
注:图中展示了 SCFAs 通过结合 GPR 受体、抑制 HDAC,进而促进 Tregs 分化和功能强化的过程,乙酸、丙酸、丁酸分别通过不同通路发挥作用
当肠道菌群紊乱(菌群失调),或者 Tregs 功能异常时,“菌群 - Treg 轴” 就会失衡,免疫系统失去控制,进而引发多种疾病。
IBD 患者的肠道菌群存在明显异常:有益的 SCFA 产生菌(如普拉梭菌、罗斯氏菌)减少,导致 SCFA 水平下降;次级胆汁酸生成不足,Tregs 功能受损,无法抑制过度炎症;同时促炎菌增多,进一步加剧肠道黏膜损伤。
更关键的是,IBD 患者的肠道 Tregs 虽然数量可能正常甚至增多,但功能严重 “失效”—— 它们无法有效抑制黏膜中的促炎细胞,导致肠道慢性炎症反复发作。
乳糜泻是对麸质的异常免疫反应,患者的肠道菌群同样存在紊乱:拟杆菌属、厚壁菌门比例异常,丙酸等抗炎代谢物减少,导致 pTregs 发育不良。同时,肠道 IL-15 过度表达,会破坏 Tregs 的抑制功能,让免疫系统对麸质产生过度反应,损伤小肠黏膜。
正常情况下,Tregs 能抑制慢性炎症,减少癌症风险;但在肿瘤微环境中,菌群失调可能导致 Tregs “叛变”—— 它们变得过度抑制,阻止免疫系统攻击肿瘤细胞,反而促进肿瘤生长。研究发现,结直肠癌患者的肠道中,丁酸产生菌减少,而促炎菌增多,Tregs 的免疫抑制功能被异常强化,加速肿瘤进展。
既然菌群 - Treg 轴对健康如此重要,我们可以通过哪些方式维持其平衡呢?
多吃富含膳食纤维的食物(如全谷物、蔬菜、豆类),为 SCFA 产生菌提供原料,促进其增殖和代谢;适量摄入富含色氨酸的食物(如鸡蛋、瘦肉、坚果),助力菌群产生抗炎的色氨酸衍生物。
补充双歧杆菌、乳酸菌等益生菌,或低聚果糖、菊粉等益生元,帮助肠道有益菌群占据优势,增强其调控 Tregs 的能力。但需注意,益生菌效果因人而异,需结合自身菌群情况选择。
对于严重菌群失调的患者,粪菌移植能将健康人的肠道菌群转移到患者体内,快速重建菌群 - Treg 轴平衡。临床研究显示,FMT 对难治性溃疡性结肠炎有一定疗效,能显著改善患者的肠道炎症。
未来可能通过补充 SCFAs、胆汁酸衍生物等代谢物,直接调控 Tregs 功能,为炎症性疾病、自身免疫病提供新的治疗方向。但目前这类疗法仍在研究中,尚未广泛应用于临床。
我们的肠道就像一个精密的 “生态系统”,肠道菌群是 “管理者”,Tregs 是 “执行者”,两者相互配合、相互依赖,共同维持免疫平衡。菌群通过结构成分、代谢产物、抗原三大 “法宝” 调控 Tregs,而 Tregs 则通过抑制过度炎症,保护菌群的多样性和稳定性。
当这个 “黄金搭档” 失衡,就可能引发炎症性肠病、乳糜泻、癌症等多种疾病;而通过饮食调节、补充益生菌、粪菌移植等方式,我们可以帮助它们重新 “握手言和”。
未来,随着对菌群 - Treg 轴机制的深入研究,我们可能会开发出更精PG电子官网准的菌群靶向疗法,让肠道这个 “免疫战场” 永远保持和平,为健康保驾护航。而现在,我们能做的就是好好呵护肠道菌群 —— 多吃膳食纤维、少吃精加工食品、避免滥用抗生素,让它们和 Tregs 一起,成为我们健康的 “最强后盾”。


